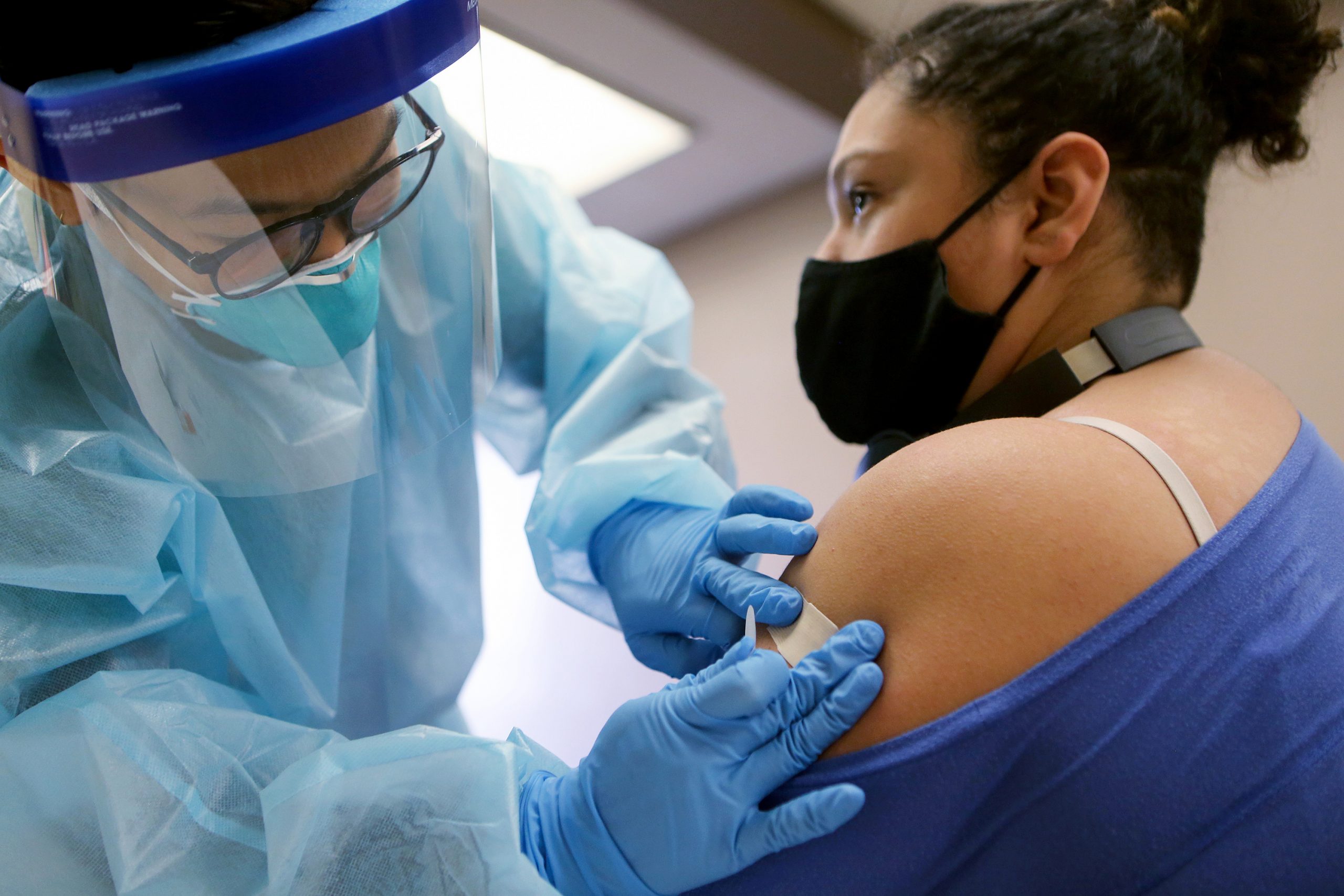
主張:新型コロナワクチンの緊急使用許可、慎重な判断を
新型コロナワクチンの開発が急速に進んでおり、治験で高い有効性を実証した企業もすでに現れている。誰もが一刻も早くワクチン接種を受けられるようにするのが望ましいことだが、「緊急使用許可」による拙速な提供はワクチンに対する信頼を損なう恐れがある。 by Clint Hermes2020.11.24
私は、新型コロナウイルス感染症(COVID-19)のワクチンを本当に欲している。多くの米国人と同様、新型コロナの症状が出たり、亡くなったりした家族や隣人が私にもいる。私の姉妹は新型コロナ病棟に配属されている看護師だが、安全な環境で仕事をしてほしいと思っている。私は医療専門の弁護士として、新型コロナワクチンに「緊急使用許可(EUA)」を出すかどうかを最終的に決定する米国食品医薬品局(FDA)の科学者を最大限に信頼している。だが、緊急使用許可を出した場合に起こるかもしれない事態を深く憂慮してもいる。
新型コロナワクチンの研究は驚くべきペースで進んでいる。開発のいずれかの段階にあるワクチン候補は200以上あり、その中にはすでに第3相試験に入っているものもいくつかある。新型コロナウイルス感染症が世界的な公衆衛生の緊急事態になってから何カ月かしかたっていないにもかかわらず、である。しかしながらFDAがワクチンを承認するには、(通常は少なくとも6カ月間、数万人の被験者の追跡を必要とする)治験を完了させる必要があるだけではない。FDAはワクチンの製造施設を視察し、詳細な製造計画や製品の安定性データを調べ、大量の治験データを詳しく調べる必要もあるのだ。このような確認作業には、ゆうに1年かそれ以上かかる。
そのためここ数カ月間、FDAは、正式承認に通常要する情報がすべて出揃う前の初期段階において、緊急使用許可により新型コロナワクチンを配布するための基準の検討を進めている。現在第3相試験を実施している製薬メーカーのうち少なくとも数社が、緊急使用許可申請の意思を公に宣言している。ファイザーは、自社ワクチンで有望な中間結果が出たのを受け、11月下旬にも申請する予定だ(日本版注:同社は11月21日に申請した)。
FDAは緊急使用許可により、公衆衛生の緊急事態において未承認の製品の利用を許可できる。FDAはこれまで、H1N1型インフルエンザやジカ熱のような感染症を対象とした診断法や治療法については慎重に緊急使用許可を出してきた。だが、緊急使用許可によってワクチンが一般市民に使用されたことはこれまで一度もない。対象範囲が広く、健康な人に接種されるという面で、ワクチンは他の医療品とは異なる。そのため、認可基準も高く設定されている。
ワクチンについてFDAに助言をする外部専門家グループ「ワ …
- 人気の記事ランキング
-
- Namibia wants to build the world’s first hydrogen economy 砂漠の国・ナミビア、 世界初「水素立国」への夢
- Promotion MITTR Emerging Technology Nite #33 バイブコーディングって何だ? 7/30イベント開催のお知らせ
- Promotion Call for entries for Innovators Under 35 Japan 2025 「Innovators Under 35 Japan」2025年度候補者募集のお知らせ
- What comes next for AI copyright lawsuits? AI著作権訴訟でメタとアンソロピックが初勝利、今後の展開は?
- Can we fix AI’s evaluation crisis? AIベンチマークはもはや限界、新たなテスト手法の登場相次ぐ
- What is vibe coding, exactly? バイブコーディングとは何か? AIに「委ねる」プログラミング新手法